ISO 13485 là tiêu chuẩn hàng đầu thế giới cho các tổ chức sản xuất, kinh doanh, dịch vụ liên quan về thiết bị y tế. Tiêu chuẩn được sử dụng trong suốt vòng đời của thiết bị y tế. Bao gồm các giai đoạn sau khi sản xuất như giao hàng, lắp đặt, dịch vụ bảo trì. Tại Việt Nam, áp dụng ISO 13485 là một trong những yêu cầu bắt buộc đối với các doanh nghiệp kinh doanh, sản xuất trong lĩnh vực trang thiết bị y tế. 2BISO là đơn vị tư vấn hàng đầu, cung cấp dịch vụ tư vấn chứng nhận ISO 13485:2016 trọn gói cho tất cả các doanh nghiệp thuộc mọi quy mô.

TƯ VẤN CHỨNG NHẬN ISO 13485:2016 TRỌN GÓI – CHI PHÍ HỢP LÝ – CAM KẾT ĐẠT CHỨNG NHẬN
Dịch vụ tư vấn trọn gói 2BISO:
✓ Tư vấn, đào tạo, cấp giấy chứng nhận
✓ Dịch vụ trọn gói từ A – Z
✓ Cam kết đạt chứng nhận
✓ Chứng nhận có giá trị toàn cầu
✓ Thời gian nghiên cứu, triển khai ISO giảm thiểu đáng kể
✓ Không phát sinh chi phí
Ưu đãi của 2BISO:
✓ Giảm ngay 10% khi đăng ký tư vấn trọn gói đồng thời từ 2 chứng chỉ: ISO 9001, ISO 14001, ISO 13485, ISO 22000, ISO 45001, HACCP, ISO 27001
Tiêu chuẩn ISO 13485 là gì?
ISO 13485 là một tiêu chuẩn quốc tế, nó đặt ra các yêu cầu đối với hệ thống quản lý chất lượng dành riêng cho ngành thiết bị y tế. ISO 13485 là một tiêu chuẩn độc lập, có phạm vi và mục đích tương tự ISO 9001. Tiêu chuẩn này bao gồm các yêu cầu bổ sung dành riêng cho các tổ chức liên quan đến thiết bị y tế.
Cũng giống các tiêu chuẩn khác của ISO, tiêu chuẩn này cũng có thể tích hợp vào các hệ thống quản lý khác của doanh nghiệp. Chứng nhận ISO 13485 chú trọng vào áp ứng các yêu cầu luật định và các yêu cầu cụ thể của khách hàng, quản lý rủi ro và duy trì các quá trình một cách hiệu quả. Ví dụ: thiết kế, sản xuất và phân phối một cách an toàn các dụng cụ y khoa
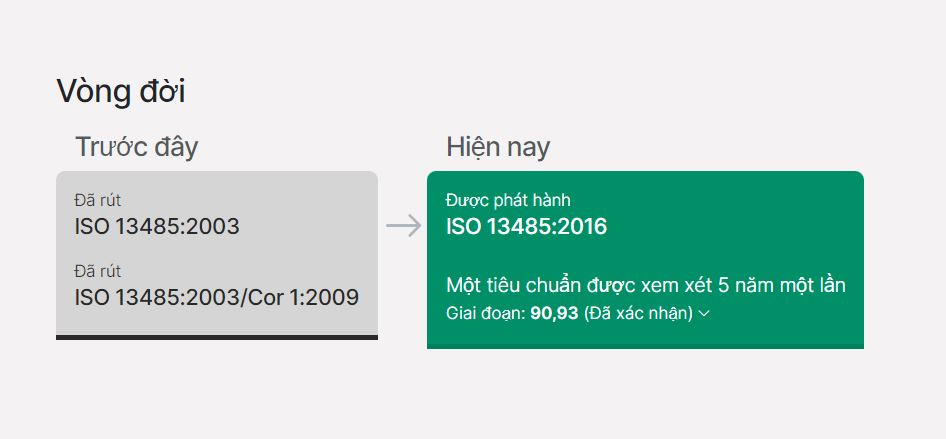
ISO 13485:2016 là phiên bản mới nhất của hệ thống quản lý chất lượng thiết bị y tế.
Chứng nhận ISO 13485:2016 theo quy định của pháp luật
Nghị định 36/2016/NĐ-CP quy định việc quản lý trang thiết bị y tế. Nghị định có hiệu lực thi hành từ ngày 01 tháng 7 năm 2016. Trong đó quy định việc áp dụng ISO 13485 là một trong những yêu cầu bắt buộc đối với các doanh nghiệp kinh doanh, sản xuất trong lĩnh vực trang thiết bị y tế. Cụ thể:
“Điều 68. Điều khoản chuyển tiếp
Cơ sở sản xuất trang thiết bị y tế đã hoạt động trước ngày Nghị định này có hiệu lực thi hành được tiếp tục hoạt động sản xuất nhưng phải hoàn thành việc công bố đủ điều kiện sản xuất trước ngày 01 tháng 7 năm 2017. Riêng đối với quy định về hệ thống quản lý chất lượng: Cơ sở sản xuất trang thiết bị y tế phải hoàn thành việc áp dụng hệ thống quản lý chất lượng ISO 9001 trước ngày 01 tháng 01 năm 2018 và hệ thống quản lý chất lượng ISO 13485 trước ngày ngày 01 tháng 01 năm 2020.”
Lợi ích khi doanh nghiệp, tổ chức được chứng nhận ISO 13485:2016
✓ Đáp ứng các yêu cầu pháp luật của cơ quan quản lý thiết bị y tế
✓ Kiểm soát, quản lý rủi ro trong sản xuất kinh doanh thiết bị y tế theo tiêu chuẩn quốc tế
✓ Cải thiện quy trình và hiệu quả quản lý chất lượng
✓ Giúp tạo ra các sản phẩm an toàn
✓ Tiết kiệm chi phí xử lý sự cố do thiết bị y tế không đáp ứng nhu cầu của khách hàng
✓ Thể hiện cam kết về tính an toàn và chất lượng thiết bị y tế
✓ Tạo dựng niềm tin với khách hàng và đối tác
✓ Mở rộng thị trường, tăng khả năng cạnh tranh cho sản phẩm.
Đối tượng áp dụng tiêu chuẩn ISO 13485:2016 – hệ thống quản lý chất lượng thiết bị y tế
ISO 13485:2016 là tiêu chuẩn được các tổ chức sử dụng trong suốt vòng đời của thiết bị y tế. Như vậy, tất cả các tổ chức, doanh nghiệp tham gia vào một hoặc nhiều công đoạn của vòng đời sản phẩm thiết bị y tế đều có thể chứng nhận ISO 13485 nếu muốn kiểm soát, vận hành và quản lý hệ thống tốt hơn theo chuẩn mực quốc tế.
Điều kiện để doanh nghiệp đạt chứng nhận ISO 13485
Điều kiện 1: Điều kiện về nhà xưởng, nhân sự
Một yêu cầu trong ISO 13485 là Doanh nghiệp pháp cần đáp ứng các yêu cầu của pháp luật.
Nghị định 36/2016/NĐ-CP có quy định về điều kiện đối với cơ sở sản xuất trang thiết bị y tế. Bao gồm:
Điều 12. Điều kiện về nhân sự của cơ sở sản xuất trang thiết bị y tế.
Điều 13. Điều kiện về cơ sở vật chất, thiết bị và quản lý chất lượng của cơ sở sản xuất trang thiết bị y tế.
Điều kiện 2: Đào tạo; xây dựng tài liệu và áp dụng tiêu chuẩn ISO 13485 vào Doanh nghiệp.
Doanh nghiệp sẽ cần thực hiện các công việc sau:
- Tìm hiểu và đào tạo tiêu chuẩn ISO 13485:2016.
- Xây dựng tài liệu; quy trình; biểu mẫu theo yêu cầu của tiêu chuẩn ISO 13485.
- Áp dụng hệ thống tài liệu, quy trình này vào doanh nghiệp.
- Duy trì vận hành hệ thống quản lý theo tiêu chuẩn ISO 13485.
Để thực hiện được những công việc này, doanh nghiệp cần có:
✓ Có nhân sự hiểu biết hoặc từng vận hành, kinh nghiệm về xây dựng áp dụng ISO 13485
✓ Lãnh đạo quyết tâm; hiểu về ISO 13485 và phải theo dõi sát việc triển khai
✓ Các đội ngũ lãnh đạo, quản lý phải dành thời gian cho việc xây dựng và áp dụng chứng nhận ISO 13485
✓ Doanh nghiệp phải có người có thể đào tạo được về ISO 13485
✓ Nguồn lực, thời gian, chi phí thực hiện phải được đáp ứng phù hợp.
Việc tự áp dụng ISO 13485 được đánh giá là rất khó khăn đối với các doanh nghiệp, đặc biệt với các doanh nghiệp nhỏ và vừa.
Để giải quyết các khó khăn khi doanh nghiệp tự áp dụng ISO. Doanh nghiệp nên tham khảo phương án thuê đơn vị tư vấn ISO 13485:2016 trọn gói. 2BISO giúp doanh nghiệp đạt được chứng nhận ISO 13485 dễ dàng và tiết kiệm hơn.
2BISO tư vấn chứng nhận ISO 13485:2016 trọn gói
Tại 2BISO chúng tôi thực hiện tư vấn trọn gói ISO 13485:2016 thông qua các bước sau:
- Bước 1: Khảo sát hiện trạng, thành lập ban ISO, thu thập thông tin, xác định phạm vi chứng nhận
- Bước 2: Tư vấn áp dụng tiêu chuẩn ISO 13485, xây dựng tài liệu, hướng dẫn áp dụng tài liệu, đánh giá nội bộ
- Bước 3: Tư vấn đánh giá ISO 13485: đăng ký chứng nhận, hỗ trợ khách hàng khắc phục nhứng điểm chưa phù hợp cho đến khi khách hàng đạt được chứng nhận ISO 13485
- Bước 4: Tư vấn khách hàng duy trì hệ thống ISO 13485
- Bước 5: Tư vấn mở rộng, thay đổi phạm vi, tái chứng nhận ISO 13485
Quý khách hàng quan tâm đến dịch vụ tư vấn chứng nhận ISO, hợp chuẩn, hợp quy, công bố chất lượng trọn gói của 2BISO xin liên hệ Hotline: 0915.347.562/0812.358.211 hoặc email: pkd@2biso.com để được hỗ trợ nhanh chóng và chính xác nhất.
CÂU HỎI THƯỜNG GẶP
Việc áp dụng ISO 13485 cung cấp nền tảng thực tế để các nhà sản xuất giải quyết Quy định về thiết bị y tế (MDR) của EU và các quy định khác, cũng như thể hiện cam kết về sự an toàn và chất lượng của thiết bị y tế.
ISO 13485 rất quan trọng đối với các nhà sản xuất thiết bị y tế vì nó cung cấp khuôn khổ để đảm bảo rằng sản phẩm của họ luôn đáp ứng các yêu cầu pháp lý và của khách hàng. Việc tuân thủ tiêu chuẩn này thể hiện cam kết của công ty trong việc sản xuất các thiết bị y tế an toàn và hiệu quả. Nó cũng giúp các công ty đáp ứng các yêu cầu pháp lý ở nhiều thị trường trên thế giới. ISO 13485 có thể giúp các công ty xác định và giảm thiểu rủi ro liên quan đến thiết kế, phát triển và sản xuất thiết bị y tế. Cuối cùng, nó có thể giúp các công ty cải thiện quy trình và tăng hiệu quả, mang lại sản phẩm tốt hơn và mức độ hài lòng của khách hàng cao hơn.
Bản sửa đổi mới nhất của ISO 13485 cho các thiết bị y tế ISO là từ tháng 3 năm 2016. Trong số các bổ sung cho bản cập nhật này bao gồm: tập trung vào rủi ro, làm rõ trách nhiệm quản lý, làm rõ trách nhiệm đào tạo, cải thiện các yêu cầu của cơ sở, điều chỉnh tốt hơn về thiết kế và yêu cầu phát triển nhiều quy định, chú trọng hơn đến việc kiểm soát nhà cung cấp, yêu cầu về thủ tục truy xuất nguồn gốc, bổ sung việc xử lý khiếu nại và nâng cao các yêu cầu về độ sạch của sản phẩm.
- Việt Nam – ISO 13485
- Châu Âu – MDR 2017/745 và ISO 13485:2016
- Vương quốc Anh – MDR Vương quốc Anh 2002
- Canada – CAN/CSA-ISO 13485:2016
- Hoa Kỳ – Quy định về hệ thống chất lượng của Hoa Kỳ (21 CFR 820), cùng với ISO 13485
- Nhật Bản – ISO 13485
- Úc – Tài liệu về Hàng hóa Trị liệu yêu cầu ISO 13485:2016.
- Singapore – ISO 13485
- Malaysia – Đạo luật về thiết bị y tế (Đạo luật 737) yêu cầu ISO 13485.
![]()

